衰老研究迎来行业地震级进展!最近,西班牙奥维耶多大学的卡洛斯·洛佩斯-奥廷(Carlos López-Otín)教授团队,在《Cell》上发表了全新的衰老标志,将原本的12大标志扩展为14个,这已经是该团队第三次更新衰老标志了。自2013年首次提出“衰老9大标志”[1], 2023年又发布了“衰老12大标志”[2],这一次,再次实现突破,更重要的是,该团队还首次提出了未来“精准衰老医学”的完整框架[3]。

下面长寿之家Changshou.com将详细解读这篇重磅研究,让我们来看看未来“精准衰老医学”将如何助力我们精准对抗衰老。
衰老的黄金标准:14大标志全新发布
什么的变化才算是衰老?
衰老这个事儿是有明确标准的。只有了解衰老的科学标志,才能制定有效的干预策略,延缓衰老进程。
根据洛佩斯-奥廷教授团队的定义,只有当生物现象严格地满足"三大铁律",才被认为是衰老标志:
• 相关性:必须与年龄增长显著相关
• 可加速性 :人为增强会加速衰老过程
• 可干预性 :人为抑制能延缓衰老过程
基于以上标准,2023年,洛佩斯-奥廷教授团队提出了衰老的12个标志,这些标志包括:基因组不稳定、端粒损耗、表观遗传改变、蛋白稳态丧失、巨自噬功能障碍、营养感应失调、线粒体功能障碍、细胞衰老、干细胞耗竭、细胞间通讯改变、慢性炎症和生态失调[2]。
如今新增加了“细胞外基质变化”和“社会心理隔离”两大特征。
从9个到14个:不断进化的认知
• 新增标志13:细胞外基质(ECM)变化
细胞外基质(extracellular matrix,ECM)是分布于细胞外空间的非细胞性物质,主要由细胞分泌的蛋白质和多糖组成,包括胶原、非胶原蛋白、弹性蛋白、糖胺聚糖和蛋白聚糖。
我们的细胞就像住在"海绵公寓"里,ECM就是支撑这些公寓的钢筋骨架。随着年龄增长,这种"海绵"会变硬、失去弹性[4]。

将长寿的裸鼹鼠的ECM关键基因移植到小鼠体内,能显著延长小鼠的健康寿命和寿命[5]。除此之外,ECM对线粒体稳态,细胞衰老,和干细胞耗竭等其他衰老标志都有很大影响[4,6,7]。
• 新增标志14:社会心理隔离
“社会心理隔离”是14个标志中唯一一个非生物标志,很多动物实验和人体临床试验的证据表明,社会心理适应是身体健康的一个基本特征。长寿之家之前的长寿指南也报道过社会孤立和孤独感会增加老人抑郁[8]、脑萎缩[9]、认知障碍[10]甚至痴呆的风险[11],还会提高老人的全因死亡风险[12],大大阻碍了老年人的长寿健康[13]。
这些衰老标志彼此之间不是孤立的,而是像"多米诺骨牌"一样相互触发。比如慢性炎症会加速端粒缩短,而端粒缩短又会加重基因组不稳定。
促衰老基因与抑衰老基因——衰老干预精准化
肿瘤和衰老,哪个更可怕?相比于癌症,大多数人或许更愿意选择健康地老去。
癌症是由于癌基因激活或抑癌基因失活引发的。自从抑癌基因被明确发现后,癌症的治疗有了新的方向,理论上可以通过抑制致癌基因(如HER2)、激活抑癌基因(如p53),或在“精准肿瘤学”领域重建肿瘤抑制机制来进行治疗。
如果癌症能够通过基因调控进行精准治疗,那么,是否也能通过调控基因来精准调节衰老呢?
精准调控“衰老开关”
这一思路其实早在去年就由作者提出,并发表于《Cell Research》上[14]。作者提出了“促衰老基因Gerogenes”和“抑衰老基因Gerosuppression”的概念,认为通过激活促衰老基因或抑衰老基因,能够加速或减缓衰老过程。

迄今为止,科学家们已经发现了多种能够影响衰老过程的基因,包括与阿尔茨海默症相关的APOE ε4和APOE ε2、调节自噬的IGF-1、减少促炎因子的FOXO3A、与早衰相关的LMNA、α-klotho,以及一些非编码RNA等。
这些基因在衰老过程中起着决定性的作用。通过精准的基因干预,能够激活或抑制这些衰老相关基因,从而调节衰老进程。
促衰老基因和抑衰老基因有两个核心条件
• 相关性:首先,它们的(表观)遗传或后遗传改变应与正常或病理性衰老密切相关;
• 可调控性:其次,干预这些基因或通路应能在动物模型中改变衰老表型,包括加速或减缓衰老、健康寿命、最大寿命等。
促衰老基因和抑衰老基因——这对“衰老开关”的发现,标志着我们正进入"量体裁衣"式的抗衰新时代——不再是笼统的"延年益寿",而是精准狙击每个人的衰老弱点。

精准衰老医学的愿景——三步走
传统老年医学就像"消防员",等老了、或疾病发生了才介入。而新兴的精准抗衰医学是提前介入,从年轻时就开始制定健康管理计划,而且还是量身定制的。
未来,精准衰老医学将分为三步走。
第一步:个性化衰老管理方案
精准衰老医学的核心在于通过系统生物学的方法,综合分析生物、临床、心理、社会和环境等因素,预测个体的健康轨迹和疾病风险,采取个性化的干预措施,以减缓、停止或逆转衰老过程。
这一理念不仅要求识别衰老过程中的潜在风险,还要能发现早期的健康变化,及时干预,避免疾病的发展。
例如,针对健康个体,精准衰老医学可以识别出潜在的病变或衰老征兆,如为APOE ε4携带者制定早期防痴呆方案;为IGF-1水平过高者制定间歇性进食计划;或为社交孤立风险高者提供心理支持和社交治疗等。
通过这样的干预措施,精准衰老医学旨在改善老年人的生活质量,并延长健康寿命。
第二步:衰老“护照”
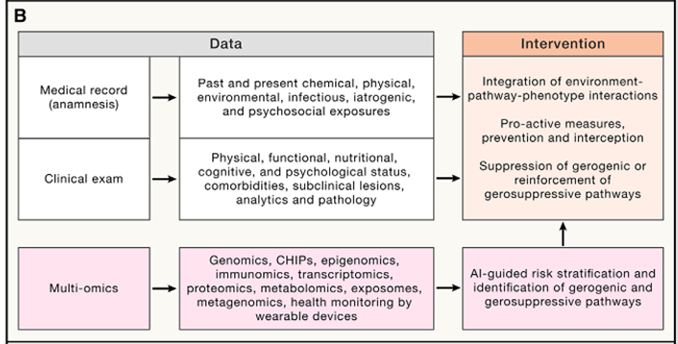
未来的精准老年医学将依赖多组学诊断,包括基因组学、代谢组学、蛋白质组学等多维度检测,制定个人衰老“护照”,精准监测衰老过程。
想象一下,未来的体检将不再只有常规的项目,可能只需要你的一滴血、或一点唾液,就能测量DNA甲基化水平,精确计算你的“生物学年龄”;分析衰老蛋白质组,检测α-Klotho等衰老相关蛋白水平;分析血液中免疫细胞组成变化,计算免疫系统年龄等等。
第三步:临床试验新蓝图
目前,许多长寿诊所推荐的治疗方法,如高压氧舱、红光疗法、冷冻疗法以及干细胞疗法等,尚未经过严格的随机、双盲3期临床试验验证其效果。因此,未来精准衰老医学干预手段的临床试验标准将更加严格。

潜在治疗策略需三期临床试验验证:1期验证安全性、2期验证疗效、3期随机双盲对照临床试验。这只是最基础的,作者针对临床试验的细节还提出了以下建议:
• 多中心平台试验,评估多个疾病的治疗方法,并应尤其关注临床健康和年龄较大的老年人群。
• 临床试验的主要终点必须是临床疗效。如衰老相关的生物标志物,认知、血糖、血压、肌肉力量等,避免使用寿命或死亡率这一较长周期的指标。
• FDA尚未认定的一些衰老临床标志物,如认知能力、运动活力、最大耗氧量、解剖学/形态学、肌肉质量等,或许将在未来成为关键的疗效评估标准。
• 如果临床试验结果成功达到预期,该结果将被纳入对照组,新的干预手段纳入实验组。
2007年,巴克衰老研究所提出了“老年科学”(geroscience)的概念[15],18年后,衰老干预的风向转向“精准衰老医学”(Precision Geromedicine),这将彻底改变我们对抗衰老的方式——从笼统的"养生建议"升级为基于个人基因、生活方式、环境因素的定制化方案。也许不久后,80岁的你还能保持50岁的活力,真正实现"优雅地老去"。
参考资料:
[1]López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M. & Kroemer, G. The hallmarks of aging. Cell 153, 1194–1217 (2013).
[2]López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M. & Kroemer, G. Hallmarks of aging: An expanding universe. Cell 186, 243–278 (2023).
[3]Kroemer, G. et al. From geroscience to precision geromedicine: Understanding and managing aging. Cell 188, 2043–2062 (2025).
[4]Mavrogonatou, E., Papadopoulou, A., Pratsinis, H. & Kletsas, D. Senescence-associated alterations in the extracellular matrix: deciphering their role in the regulation of cellular function. AJP Cell Physiology 325, C633–C647 (2023).
[5]Zhang, Z. et al. Increased hyaluronan by naked mole-rat Has2 improves healthspan in mice. Nature 621, 196–205 (2023).
[6]Zhang, H. et al. The extracellular matrix integrates mitochondrial homeostasis. Cell 187, 4289-4304.e26 (2024).
[7]Barakat, N. et al. Inhibition of metalloproteinases extends longevity and function of in vitro human IPSC-Derived skeletal muscle. Biomedicines 12, 856 (2024).
[8]Joel Salinas, Alexa S. Beiser, et al. Association of loneliness with 10-Year dementia risk and early markers of vulnerability for neurocognitive decline. Neurology. 2022, 98 (13): e1337-e1348.
[9]Hirabayashi N, Honda T, Hata J, et al. Association between frequency of social contact and brain atrophy in Community-Dwelling Older People without Dementia. Neurology. 2023;101(11).
[10]Huang Y, Zhu X, Liu X, Li J. The effects of loneliness, social isolation, and associated gender differences on the risk of developing cognitive impairment for Chinese oldest old. Aging & Mental Health. 2022;27(7):1360-1367.
[11]Saul H, Gursul D. Loneliness is strongly linked to depression among older adults, a long term study suggests. BMJ. October 2021:n2524.
[12]Kammar-García A, Ramírez-Aldana R, Roa-Rojas P, et al. Association of loneliness and social isolation with all-cause mortality among older Mexican adults in the Mexican health and aging study: a retrospective observational study. BMC Geriatrics. 2023;23(1).
[13]Li Y, Jigeer G, Lv Y, et al. Social isolation and likelihood of becoming centenarians: evidence from the Chinese longitudinal healthy longevity survey. BMC Geriatrics. 2024;24(1).
[14]López-Otín, C., Maier, A. B. & Kroemer, G. Gerogenes and gerosuppression: the pillars of precision geromedicine. Cell Research 34, 463–466 (2024).
[15]Buck Institute. Buck Institute awarded $25 million to establish new scientific discipline of geroscience - BUCK.
